एंटीबायोटिक्स दवाएं क्या है,और कैसे काम करती है ?

एंटीबायोटिक्स दवाएं क्या है
एंटीबायोटिक्स दवाएं क्या है,और कैसे काम करती है ?
एंटीबायोटिक्स दवाएं बैक्टीरिया के कारण होने वाले संक्रमण को रोकने में मदद करती हैं। एंटीबायोटिक्स दवाएं बैक्टीरिया को मारकर प्रजनन करने से रोकते हैं। एंटीबायोटिक शब्द का अर्थ है “जीवन के विरुद्ध।” आपके शरीर में कीटाणुओं को मारने वाली कोई भी दवा तकनीकी रूप से एक एंटीबायोटिक है। लेकिन अधिकांश लोग इस शब्द का उपयोग तब करते हैं जब वे उस दवा के बारे में बात करते हैं जो बैक्टीरिया को मारने के लिए होती है। इससे पहले कि वैज्ञानिकों ने 1920 के दशक में पहली बार एंटीबायोटिक्स की खोज की, स्ट्रेप गले की तरह कई लोग मामूली जीवाणु संक्रमण से मर गए। सर्जरी जोखिम भरा था, भी। लेकिन 1940 के दशक में एंटीबायोटिक उपलब्ध होने के बाद, जीवन प्रत्याशा में वृद्धि हुई, सर्जरी सुरक्षित हो गई, और लोग जीवित रह सकते थे जो घातक संक्रमण हुआ करते थे।

एंटीबायोटिक्स क्या है?
एंटीबायोटिक्स को एंटीबैक्टिरियल भी कहा जाता है। बैक्टेरियल इंफैक्शन्स से लड़ने के लिए यह बहुत ही शक्तिशाली दवा है। यह अगर उचित तरीके लिया जाय को आपके जीवन को बचा सकता है। लेकिन दूसरी दवा की तरह एंटीबायोटिक्स का भी साइड इफैक्ट होता है।
एंटीबायोटिक्स कैसे कार्य करते है ?
आपके शरीर में रहने वाले अधिकांश बैक्टीरिया आपको हानि नही पहुचाते है । कुछ बैक्टीरिया मददगार भी होते है , बैक्टीरिया लगभग किसी भी अंग को संक्रमित कर सकते हैं। एंटीबायोटिक्स आमतौर पर मदद कर सकते हैं। ये संक्रमण के प्रकार हैं जिन्हें एंटीबायोटिक दवाओं के साथ इलाज किया जा सकता है:
- कुछ कान और साइनस संक्रमण
- दंत संक्रमण
- त्वचा में संक्रमण
- मेनिनजाइटिस (मस्तिष्क और रीढ़ की हड्डी की सूजन)
- खराब गला
- मूत्राशय और गुर्दे में संक्रमण
- बैक्टीरियल निमोनिया
- काली खांसी
एंटीबायोटिक दवाओं के साथ केवल जीवाणु संक्रमण को मारा जा सकता है। सामान्य सर्दी, फ्लू, अधिकांश खांसी, कुछ ब्रोंकाइटिस संक्रमण, सबसे अधिक गले में खराश, और पेट फ्लू सभी वायरस के कारण होते हैं। एंटीबायोटिक्स ने उनके इलाज के लिए काम नहीं किया। आपका डॉक्टर आपको बताएगा कि आप इन बीमारियों को खत्म करने के लिए या इनसे छुटकारा पाने में मदद करने के लिए एंटीवायरल ड्रग्स का सेवन करें। यह हमेशा जरूरी नहीं होता है कि कोई संक्रमण वायरल है या बैक्टीरिया से। कभी-कभी आपका डॉक्टर यह तय करने से पहले परीक्षण करेगा कि आपको किस उपचार की आवश्यकता है। कुछ एंटीबायोटिक्स कई अलग-अलग प्रकार के जीवाणुओं पर काम करते हैं। उन्हें “ब्रॉड-स्पेक्ट्रम” कहा जाता है, अन्य केवल विशिष्ट बैक्टीरिया को लक्षित करते हैं। उन्हें “संकीर्ण-वर्णक्रम” के रूप में जाना जाता है।
एंटीबायोटिक्स के दुष्प्रभाव
एंटीबायोटिक्स अक्सर आपके पाचन तंत्र को प्रभावित करते हैं, जबकि वे एक संक्रमण का इलाज कर रहे हैं। आम दुष्प्रभावों में शामिल हैं:
- उल्टी
- जी मिचलाना
- दस्त
- सूजन या अपच
- पेट में दर्द
- भूख में कमी
कभी-कभी, आपके अन्य लक्षण हो सकते हैं, जैसे:
- पित्ती – एक उठाया, खुजली वाली त्वचा लाल चकत्ते
- खाँसना
- घरघराहट
- तंग गले या सांस लेने में परेशानी
इन लक्षणों का मतलब हो सकता है कि आपको अपने एंटीबायोटिक से एलर्जी है, इसलिए यदि आपके पास है तो अपने डॉक्टर को तुरंत बताएं। यदि आप गर्भनिरोधक गोलियां ले रहे हैं, तो एंटीबायोटिक्स उन्हें काम करने से रोक सकती हैं और साथ ही उन्हें चाहिए, इसलिए अपने डॉक्टर से बात करें कि क्या वैकल्पिक जन्म नियंत्रण विधियां एक अच्छा विचार हो सकता है। एंटीबायोटिक्स लेते समय महिलाओं को योनि खमीर संक्रमण भी हो सकता है। लक्षणों में खुजली, जलन, योनि स्राव (कॉटेज पनीर के समान दिखता है) और सेक्स के दौरान दर्द शामिल हैं। इसका इलाज एक एंटी-फंगल क्रीम के साथ किया जाता है।

एंटीबायोटिक प्रतिरोध एंटीबायोटिक्स एक शक्तिशाली रोगाणु से लड़ने वाले उपकरण हैं जब सावधानीपूर्वक और सुरक्षित रूप से उपयोग किए जाते हैं। लेकिन सभी एंटीबायोटिक के आधे से एक तक का उपयोग आवश्यक नहीं है। अति प्रयोग ने जीवाणुरोधी प्रतिरोध किया है। बैक्टीरिया समय के साथ अनुकूलित होते हैं और “सुपर बैक्टीरिया” या “सुपरबग्स” बन जाते हैं। वे बदल जाते हैं ताकि एंटीबायोटिक्स अब उन पर काम न करें। वे एक बड़ा खतरा पैदा करते हैं, क्योंकि उन्हें मारने के लिए कोई दवा नहीं है। सुपर बैक्टीरिया के प्रसार को धीमा करने में मदद करने का सबसे अच्छा तरीका एंटीबायोटिक्स के साथ स्मार्ट होना है। ऐसे:
- अपने चिकित्सक पर विश्वास करें यदि वह कहती है कि आपको उनकी आवश्यकता नहीं है।
- वायरल संक्रमण के लिए उन्हें न लें।
- केवल वही लें जो आपके डॉक्टर ने आपके लिए निर्धारित किया है।
- उन्हें निर्देशित के रूप में ले लो।
- खुराक मत छोड़ो।
- अपने चिकित्सक द्वारा निर्धारित दिनों की पूरी संख्या के लिए उन्हें ले लो।
- बाद के लिए उन्हें न सहेजें।
एंटीबायोटिक्स का उपयोग
- एंटीबायोटिक्स डॉक्टर की सलाह के बगैर न लें। हर बीमारी के लिए अलग प्रकार के एंटीबायोटिक्स होते हैं, जिसे डॉक्टर की सलाह से ही समझ सकते हैं।
- जितनी मात्रा में और जिस समय डॉक्टर बताएं, उसी अनुसार एंटीबायोटिक्स लें, क्योंकि बताई गई मात्रा और समय का ध्यान न रखना नुकसान पहुंचा सकता है।
- डॉक्टर जितने समय के लिए एंटीबायोटिक्स कोर्स करने की सलाह दें, उसे अवश्य पूरा करें, तबीयत ठीक लगने पर बीच में ही इनका सेवन बंद न कर दें।
- अगर आप उपचार तुरंत बंद कर देंगे तो कुछ बैक्टीरिया जीवित बच जाएंगे और आपको पुन: संक्रमित कर देंगे।
- हर इंसान के शरीर के मुताबिक अलग एंटीबायोटिक्स लाभ देते हैं, इसलिए किसी दूसरे व्यक्ति के लिए दिए गए एंटीबायोटिक्स का सेवन कतई न करें।
- इन्हें खाना खाने से एक घंटा पहले या दो घंटे बाद लेना चाहिए।
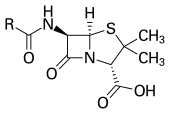
आम उपयोग में, प्रतिजैविक या एंटीबायोटिक एक पदार्थ या यौगिक है, जो जीवाणु को मार डालता है या उसके विकास को रोकता है। प्रतिजैविक रोगाणुरोधी यौगिकों का व्यापक समूह होता है, जिसका उपयोग कवक और प्रोटोजोआ सहित सूक्ष्मदर्शी द्वारा देखे जाने वाले जीवाणुओं के कारण हुए संक्रमण के इलाज के लिए होता है।
“एंटीबायोटिक” शब्द का प्रयोग 1942 में सेलमैन वाक्समैन द्वारा किसी एक सूक्ष्म जीव द्वारा उत्पन्न किये गये ठोस या तरल पदार्थ के लिए किया गया, जो उच्च तनुकरण में अन्य सूक्ष्मजीवों के विकास के विरोधी होते हैं। इस मूल परिभाषा में प्राकृतिक रूप से प्राप्त होने वाले ठोस या तरल पदार्थ नहीं हैं, जो जीवाणुओं को मारने में सक्षम होते हैं, पर सूक्ष्मजीवों (जैसे गैस्ट्रिक रसऔर हाइड्रोजन पैराक्साइड) द्वारा उत्पन्न नहीं किये जाते और इनमें सल्फोनामाइड जैसे सिंथेटिक जीवाणुरोधी यौगिक भी नहीं होते हैं। कई प्रतिजैविक अपेक्षाकृत छोटे अणु होते हैं, जिनका भार 2000 Da से भी कम होता हैं।
औषधीय रसायन विज्ञान की प्रगति के साथ-साथ अब अधिकतर एंटीबायोटिक्ससेमी सिंथेटिकही हैं, जिन्हें प्रकृति में पाये जाने वाले मूल यौगिकों से रासायनिक रूप से संशोधित किया जाता है, जैसा कि बीटालैक्टम (जिसमें पेनसिलियम, सीफालॉसपोरिन और कारबॉपेनम्स के कवक द्वारा उत्पादितपेनसिलिंस भी शामिल हैं) के मामले में होता है। कुछ प्रतिजैविक दवाओं का उत्पादन अभी भी अमीनोग्लाइकोसाइडजैसे जीवित जीवों के जरिये होता है और उन्हें अलग-थलग रख्ना जाता है और अन्य पूरी तरह कृत्रिम तरीकों- जैसे सल्फोनामाइड्स,क्वीनोलोंसऔरऑक्साजोलाइडिनोंससे बनाये जाते हैं। उत्पत्ति पर आधारित इस वर्गीकरण- प्राकृतिक, सेमीसिंथेटिक और सिंथेटिक के अतिरिक्त सूक्ष्मजीवों पर उनके प्रभाव के अनुसार प्रतिजैविक को मोटे तौर पर दो समूहों में विभाजित किया जा सकता हैं: एक तो वे, जो जीवाणुओं को मारते हैं, उन्हें जीवाणुनाशक एजेंट कहा जाता है और जो बैक्टीरिया के विकास को दुर्बल करते हैं, उन्हें बैक्टीरियोस्टेटिक एजेंट कहा जाता है।
प्रतिजैविक दवाओं का इतिहास
बीसवीं सदी की शुरुआत से पहले कई संक्रामक रोगों के इलाजऔषधीय लोकोक्तियों पर आधारित होते थे। प्राचीन चीनी चिकित्सा में संक्रमण के इलाज के लिए पौधों से प्राप्त प्रतिजैविक तत्वों का उपयोग 2,500 साल पहले शुरू हुआ। प्राचीन मिस्र,प्राचीन यूनानी और मध्ययुगीन अरब जैसी कई प्राचीन सभ्यताओं में संक्रमण के इलाज के लिए फफूंद और पौधों का इस्तेमाल होता था। 17 वीं सदी मेंकुनैन की छाल का उपयोग मलेरिया के इलाज के लिए व्यापक रूप से होता था, जो रोगजीनस प्लासमोडियम के प्रोटोजोन परजीवी के कारण होता है। बीमारियां क्यों होती हैं, यह जानने-समझने के वैज्ञानिक प्रयासों, सिंथेटिक प्रतिजैविक कीमोथेरेपी के विकास और प्राकृतिक प्रतिजैविक दवाओं का पृथक्करण प्रतिजैविक के विकास में मील के पत्थर साबित हुए.
मूलतः एंटीबायोसिस कहे जाने वाले प्रतिजैविक वैसी दवाएं हैं, जो बैक्टीरिया के खिलाफ काम करती हैं। एंटीबायोसिस शब्द का मतलब है “जीवन के खिलाफ” और इसकी शुरुआत फ्रांस के जीवाणु विज्ञानीविलेमिन ने इन दवाओं के असर का वर्णन करने के लिए की. (एंटीबायोसिस का पहली बार वर्णन 1877 में बैक्टीरिया में किया गया था, जब लुईस पाश्चर और रॉबर्ट कोच ने देखा कि हवा से पैदा हुए एक बैसिलस द्वारा बैसीलस एंथ्रासिस के विकास को रोका जा सकता है। इन दवाओं को बाद में अमेरिकी सूक्ष्मजीव विज्ञानी सेलमैन वाक्समैन ने 1942 में प्रतिजैविक नाम दिया.
एक विज्ञान के रूप में सिंथेटिक प्रतिजैविक कीमोथेरेपी और प्रतिजैविक के विकास की कहानी 1880 के दशक के आखिर में जर्मनी में वहां के चिकित्सा विज्ञानी पॉल एर्लीच ने शुरू की. डॉ॰ एर्लीच ने बताया कि कुछ रंग मानव, पशु या बैक्टीरियल कोशिकाओं को बांधने व रंगने में सक्षम होते हैं, जबकि दूसरे ऐसा ऐसा नहीं कर पाते. बाद में उन्होंने यह विचार व्यक्त किया कि संभव है कि कुछ रंग या रसायन जादुई गोली या चुनिंदा दवा के रूप में काम करें और वे मानव मेजबान को नुकसान पहुंचाए बिना बैक्टीरिया को बांधकर मार दें. काफी प्रयोगों और विभिन्न सूक्ष्म जीवों के खिलाफ रंगों के प्रदर्शन के बाद उन्होंने चिकित्सकीय रूप से उपयोगी दवा, मानव निर्मित प्रतिजैविक सालवर्सनकी खोज की.हालांकि, पार्श्व कुप्रभाव (साइड इफेक्ट) और बाद में प्रतिजैविक पेनिसिलिन की खोज के बाद सालवर्सन का प्रतिजैविक के रूप में इस्तेमाल खत्म हो गया। एर्लीच के कार्यों, जिससे प्रतिजैविक क्रांति का जन्म हुआ, के बाद 1932 में डोमेक ने प्रोन्टोसिल की खोज की पहले व्यावसायिक रूप से उपलब्ध जीवाणुरोधी प्रतिजैविक प्रोंटोसिल का विकास गेरहर्ड डोमेक (जिन्हें उनके प्रयासों के लिए 1939 में चिकित्सा के क्षेत्र में नोबेल पुरस्कार मिला) की अगुवाई वाली एक टीम ने जर्मनी के IG फारबेन कांग्लोमरेट केबेयर प्रयोगशालाओं में किया। प्रोन्टोसिल का ग्रैम पोजिटिव कोकी पर अपेक्षाकृत व्यापक प्रभाव दिखा और यह इंट्रोबैक्टीरिया के खिलाफ भी नहीं था। इस पहली सल्फोनामाइड दवा के विकास से प्रतिजैविक दवाओं के युग की शुरुआत हुई.
प्राकृतिक सूक्ष्मजीवों द्वारा उत्पादित प्रतिजैविक दवाओं की खोज सूक्ष्म जीवों के बीच एंटीबायोसिस के निरीक्षण पर पहले किये गये काम से प्रभावित थी। पाश्चर ने कहा ‘कि अगर हम कुछ बैक्टीरिया के बीच परस्पर विरोध की प्रक्रिया में हस्तक्षेप कर सकते हैं तो इससे ‘शायद चिकित्सा विज्ञान के लिए काफी उम्मीदें पैदा होंगी. पेनिसिलियम spp के बैक्टीरिया के परस्पर विरोध का सबसे पहला वर्णन जॉन टिंडान ने 1875 में इंग्लैंड में किया। हालांकि, उनके काम पर 1928 में अलेक्जेंडर फ्लेमिंग द्वारा पेनिसिलिन की खोज किये जाने तक वैज्ञानिक समुदाय ने ज्यादा ध्यान नहीं दिया. यहां तक कि तब पेनिसिलिन की चिकित्सीय क्षमता पर पूरा विश्वास नहीं था। उसके दस साल बाद, अर्नस्ट चेन और हावर्ड फ्लोरे ने बी. ब्रेविस द्वारा खोजे गये व जर्मिसिडिन नाम दिये गये एक अन्य प्राकृतिक प्रतिजैविक पदार्थ की खोज के बाद फ्लेमिंग के काम में रुचि ली. 1939 में, रेने डुबोस को जर्मिसिडिन को द्वितीय विश्व युद्ध के दौरान घाव और अल्सर के इलाज में प्रयोग की गयी पहली व्यावसायिक रूप से उत्पादित प्रतिजैविक दवा के रूप में कारगर साबित होने के रूप में अलग पहचान मिली. फ्लोरे और चैन ने पेनिसिलिन को शुद्ध करने में कामयाबी पाई. इस शुद्ध किये गये प्रतिजैविक ने जीवाणुओं की एक विस्तृत श्रृंखला के खिलाफ जीवाणुरोधी गतिविधि का प्रदर्शन किया। इसमें विषाक्तता भी कम थी और प्रतिकूल प्रभाव पैदा किये बिना इन्हें लिया जा सकता था। इसके अलावा, इसकी गतिविधि मवाद जैसे जैविक घटकों से अवरुद्ध नहीं होती थी, जैसा कि उस समय उपलब्ध सिंथेटिक प्रतिजैविक सल्फोनामाइड के प्रयोग से होता था। इतनी ताकतवर प्रतिजैविक की खोज अभूतपूर्व थी। पेनसिलिन के विकास ने समान क्षमताओं वाले प्रतिजैविक यौगिकों की खोज के प्रति नई रुचि पैदा की. पेनिसिलिन की उनकी खोज के कारण अर्नस्ट चेन, हावर्ड फ्लोरे को 1945 में संयुक्त रूप से नोबेल पुरस्कार प्रदान किया गया। फ्लोरे ने पूरी दृढता से और व्यवस्थित रूप से जीवाणुरोधी यौगिकों की खोज प्रारंभ करने का श्रेय डुबोस को दिया. इसी तरह की पद्धति की वजह से जर्मिसिडिन की खोज हुई, जिसने पेनिसिलिन में फ्लोरे की खोज को पुनर्जीवित किया।
रोगाणुरोधी फर्माकोडिइनामिक्स
रोगाणुरोधी चिकित्सा के सफल परिणाम के लिए एक प्रतिजैविक की गतिविधियों का मूल्यांकन महत्वपूर्ण है। गैर-सूक्ष्मदर्शी विषाणुओं के कारक, जैसे मेजबान प्रतिरोधी क्षमता तंत्र, संक्रमण का स्थान, बीमारी के रूप में मौजूद साथ-साथ आंतरिक फर्माकोकिनेटिक और फर्माकोडिनेमिक प्रतिजैविक के सूक्ष्म घटक हैं। मूल रूप से प्रतिजैविक दवाओं का वर्गीकरण ऐसे हो सकता है कि जो जीवाणुओं के खिलाफ घातक या जीवाणुनाशक कार्रवाई करते हैं या वे जो बैक्टीरियोस्टेटिक है, जिनका काम जीवाणुओं की वृद्धि को रोकना है। प्रतिजैविक दवाओं की जीवाणुनाशक गतिविधि उनके चरणबद्ध विकास पर निर्भर है और सभी नहीं, लेकिन ज्यादातर मामलों में दवा की “विनाशक” क्षमता के लिए जीवाणुनाशक प्रतिजैविक दवाओं की कार्रवाई के दौरान कोशिकाओं के विभाजन की आवश्यकता होती है।] ये वर्गीकरण प्रयोगशाला में दिखे व्यवहार पर आधारित है; व्यावहारिक रूप से ये दोनों एक जीवाणु के संक्रमण को खत्म करने में सक्षम हैं। प्रतिजैविक दवाओं की कार्रवाई के ‘इन विट्रो (In vitro) गतिविधि के लक्षण की जानकारी, गतिविधि मूल्यांकन के लिए रोगाणुरोधी की न्यूनतम निरोधात्मक एकाग्रता व रोगाणुरोधी शक्ति रोगाणुरोधक क्षमता के उत्कृष्ट संकेतक हैं। हालांकि, चिकित्सकीय गतिविधि में, अकेले ये कदम निदानमूलक परिणामों की भविष्यवाणी के लिए अपर्याप्त हैं। रोगाणुरोधी गतिविधि के साथ किसी प्रतिजैविक के फर्माकोकिनेटिक प्रोफ़ाइल के संयोजन द्वारा कई फर्माकोलोजिकल पैरामीटर में दवा की प्रभावशीलता के महत्वपूर्ण चिन्ह दिखते हैं। प्रतिजैविक दवाओं की गतिविधि एकाग्रता पर निर्भर है और उनकी रोगाणुरोधी गतिविधि उत्तरोत्तर रोगाणुरोधी प्रतिजैविक सांद्रता के साथ बढ़ती जाती है। वे भी समय पर आधारित हो सकते हैं, जहां उनकी रोगाणुरोधी गतिविधि में वृद्धि प्रतिजैविक सांद्रता की वृद्धि के साथ नहीं होती, हालांकि, यह भी महत्वपूर्ण है कि एक खास अवधि के लिए न्यूनतम निरोधात्मक एकाग्रता सीरम को बरकरार रखा जाये. कर्विस मारने के लिए उपयोग किये जाने वाले प्रतिजैविक के मारक तत्वों का प्रयोगशाला मूल्यांकन करना समय निर्धारण या एकाग्रता पर आधारित एक्टीमाइक्रोबायल गतिविधि के निर्धारण में उपयोगी है।
प्रतिजैविक श्रेणियां
आमतौर पर प्रतिजैविक दवाओं का वर्गीकरण उनकी कार्रवाई के तंत्र, रासायनिक संरचना या गतिविधि के स्पेक्ट्रम के आधार पर होता है। अधिकांश प्रतिजैविक बैक्टीरिया के कार्य या उनकी विकास प्रक्रिया पर निशाना साधते हैं। प्रतिजैविक दवाएं, जो बैक्टीरिया की कोशिका दीवार (पेनसिलिन्स, सेफ़्लोस्पोरिन्स) या कोशिका झिल्ली (polymixins), या आवश्यक जीवाणु एंजाइम (quinolones, sulfonamides) पर लक्ष्य केंद्रित करती हैं, सामान्यत: जीवाणुनाशक प्रकृति की होती हैं। वे, जो प्रोटीन सिंथेसिस, जैसे अमीनोग्लाइकोसाइडस, माइक्रोलाइडस और टेट्रासाइक्लिन्स पर निशाना साधते हैं, आमतौर पर बैक्टीरियोस्टैटिक होते हैं इसके अलावा अपने लक्ष्य की खासियत पर आधारित वर्गीकरण भी होता है: जैसे “संकुचित स्पेक्ट्रम प्रतिजैविक” विशेष प्रकार के जीवाणुओं, जैसे ग्रैम निगेटिव, या ग्रैम पॉजिटिव जीवाणु पर लक्ष्य साधते हैं, जबकि व्यापक स्पेक्ट्रम प्रतिजैविक जीवाणुओं की एक विस्तृत श्रृंखला को प्रभावित करते हैं। पिछले कुछ वर्षों में प्रतिजैविक दवाओं के तीन नए वर्ग निदान के लिए इस्तेमाल किये जा रहे हैं। इस तरह प्रतिजैविक यौगिकों के नए वर्गों की खोज में 40 सालों का समय लगा है। इन नई प्रतिजैविक दवाओं के निम्नलिखित तीन वर्ग हैं: साइक्लिक लिपोपेपटाइडस (डेप्टोमाइसिन), ग्लीसाइलसीक्लाइंस (टीगेसाइक्लिन), और ओक्साजोलाइडिनोंस (लाइनेजोलिड). टीगेसाइक्लिन एक व्यापक स्पेक्ट्रम प्रतिजैविक है, जबकि दो अन्य का उपयोग ग्रैम-पॉजिटिव संक्रमण के इलाज के लिए होता है। इन घटनाओं को वर्तमान प्रतिजैविक दवाओं की बैक्टीरिया प्रतिरोधक प्रतिक्रिया मापने के साधन की उम्मीद के रूप में देखा जा सकता है।
उत्पादन
1939 में पहली बार फ्लोरे और चैन के अहम प्रयासों के बाद से चिकित्सा में प्रतिजैविक दवाओं के महत्व के कारण इनकी खोज और उत्पादन के लिए शोध की प्रेरणा मिली है। उत्पादन की प्रक्रिया में सामान्यतः सूक्ष्मजीवों की व्यापक श्रेणियों का निरीक्षण और उनका परीक्षण तथा संशोधन शामिल होता है। उत्पादन किण्वन (फर्मेंटेशन) के जरिये, आमतौर पर मजबूत एरोबिक तरीके से किया जाता है।
प्रशासन
मौखिक प्रतिजैविक को निगलकर लिया जाता है, जबकि नसों के जरिये दिये जाने वाले प्रतिजैविक और ज्यादा गंभीर मामलों, जैसे गहराई तक फैले प्रणालीगत संक्रमणों में इस्तेमाल किये जाते हैं। प्रतिजैविक का प्रयोग कभी-कभी बाहर से भी किया जाता है, जैसे आंख में डाली जाने वाली दवाएं या मरहम.
दुष्प्रभाव
हालांकि आमतौर पर प्रतिजैविक दवाओं को सुरक्षित और अच्छी तरह सहन करने योग्य माना जाता है, पर ये व्यापक रूप से प्रतिकूल प्रभाव से भी जुड़ी हुई हैं। दुष्प्रभाव कई तरह के, विविध रूपों वाले और पूरी तरह प्रतिजैविक के उपयोग और लक्ष्यित किये जाने वाले सूक्ष्मजीवों पर निर्भर होते हैं। नई दवाओं से उपचार के सुरक्षा प्रोफाइल कई वर्षों से उपयोग की जा रही दवाओं जितने स्थापित नहीं है। प्रतिकूल प्रभाव बुखार और मिचली से लेकर फोटोडर्माटाइटिस और एनाफिलिक्स जैसे बड़े एलर्जी तक के रूप में दिख सकते हैं। आम रूप से दिखने वाले दुष्प्रभावों में से एकदस्त है, जो कभी-कभी एनेरोबिक बैक्टीरियम क्लोस्ट्रिडियम डिफिसाइल के कारण होते हैं और यह प्रतिजैविक द्वारा आंत के फ्लोरा के सामान्य संतुलन को अस्तव्यस्त करने से होता है। रोग पैदा करने वाले बैक्टीरिया की इस तरह अतिवृद्धि को प्रतिजैविक लेने के दौरान प्रो-बायोटिक की खुराक लेने खत्म किया जा सकता है। प्रतिजैविक के कारण उन जीवाणुओं की संख्या भी बढ़ सकती है जो सामान्य रूप से योनि के फ्लोरा के घटक के रूप में उपस्थित होते हैं और इससे वोल्वों-योनि क्षेत्र में जीनस कैंडीडा खमीर की प्रजातियों का जरूरत से ज्यादा विकास हो सकता है। दूसरी दवाओं के साथ अंतरक्रियाशीलता से दूसरे पार्श्व कुप्रभावों भी दिख सकते हैं, जैसे प्रणालीगत कोर्टीकोस्टेरायड के साथ एक क्विनोलोन प्रतिजैविक लेने से कण्डरा (मांशपेशी को हडडी से जोड़ने वाली नस) की क्षति का जोखिम बढ़ जाता है।
औषधि-औषधि अंतरक्रियाएं
गर्भनिरोधक गोलियां
अनुमान किया जाता है कि जन्म नियंत्रण गोलियों की प्रभावशीलता के साथ कुछ प्रतिजैविक दवाओं का हस्तक्षेप दो तरीकों से होता है। आंत्र फ्लोरा में संशोधन से एस्ट्रोजेन्स के अवशोषण में कमी आ सकती है। दूसरे, हेप्टिक लीवर एंजाइम लेने से गोली के सक्रिय तत्वों का चयापचयन (मेटाबोलाइज) तेज होता है और इससे गोली की उपयोगिता प्रभावित हो सकती हैं। हालांकि ज्यादातर अध्ययनों के जरिये यह संकेत मिलता है कि प्रतिजैविक दवाएं गर्भनिरोधकों के काम में हस्तक्षेप नहीं करती हैं। हालांकि कुछ प्रतिशत महिलाएं प्रतिजैविक लेने के दौरान जन्म नियंत्रण गोलियों के कम प्रभाव पड़ने की अनुभूति करती हैं, जबकि असफलता की दर की तुलना गोली लेने वाली महिलाओं से की जा सकती है। इसके अलावा, कोई अन्य अध्ययन नहीं दिखता है, जिससे अंतिम तौर पर पता चले कि पेट के फ्लोरा में व्यवधान गर्भनिरोधक को प्रभावित करता है। ऐंटीफंगल दवा ग्रीसोफुल्विन और व्यापक दायरे वाले प्रतिजैविक रिफैम्पिसिन द्वारा यकृत एंजाइमों के अधिष्ठापन के माध्यम से मौखिक गर्भनिरोधक गोली लेने से ऐसा हो सकता है। इसलिए सिफारिश की जाती है कि इन एंटीमाइक्रोबियल्स के प्रयोग से रोगाणुरोधी चिकित्सा के दौरान अतिरिक्त गर्भनिरोधक उपायों का सहारा लेना चाहिए.
शराब
शराब प्रतिजैविक दवाओं की गतिविधि या चयापचयन में दखल दे सकती है इससे यकृत एंजाइम की गतिविधि प्रभावित हो सकती है, जिससे प्रतिजैविक दवाओं का प्रभाव खत्म हो जाता है। इसके अलावा, मेट्रोनिडाजोल, टिनिडाजोल, सीफामैंडोल, केटेकोनाजोल, लैटमोक्सेफ, सीफोप्राजोन, सेफमेनोक्साइम और फुराजोलिडिन जैसे कुछ प्रतिजैविक अल्कोहल के साथ प्रतिक्रिया करते हैं, जिससे गंभीर पार्श्व कुप्रभाव, जिनमें उल्टी, मिचली और सांस की तकलीफ शामिल है, दिखते हैं। इसलिए ऐसे प्रतिजैविक लेने के दौरान शराब का सेवन नहीं करना चाहिए. इसके अतिरिक्त, शराब के सेवन से कुछ खास परिस्थितियों में डोक्सीसाइक्लिन और इरिथ्रोमाइसिन सुसीनेट के सीरम स्तर में कमी हो सकती है।
प्रतिजैविक प्रतिरोध
प्रतिजैविक प्रतिरोध का उद्भव एक विकासशील प्रक्रिया है, जो जीव के चयन पर आधारित है और जिससे प्रतिजैविक दवाओं की खुराक के लिए जीवित रहने की क्षमता में वृद्धि हुई है, जो पहले घातक होता था। पेनिसिलिन और इरीथ्रोमाइसीन जैसे प्रतिजैविक, जो एक समय चमत्कारी इलाज माने जाते थे, अब कम प्रभावकारी दिख रहे हैं, क्योंकि जीवाणु अधिक प्रतिरोधी बन रहे हैं। प्रतिजैविक खुद एक चयनात्मक दबाव के रूप में काम करते हैं, जो एक निश्चित संख्या में प्रतिरोधी जीवाणुओं के विकास की अनुमति देते हैं और फिर सरलता से नष्ट होने वाले जीवाणुओं को जीवित रखते हैं। 1943 में लुरिया-डेलब्रुक प्रयोग के जरिये जीवाणुओं की आबादी के भीतर पहले से मौजूद प्रतिजैविक प्रतिरोधी उत्परिवर्ती जीव का प्रदर्शन किया गया। जीवाणु का जीवन अक्सर विरासत में मिले प्रतिरोध का परिणाम होता है। कोई भी प्रतिजैविक प्रतिरोध एक जैविक कीमत मांगता है और प्रतिजैविक प्रतिरोधी जीवाणुओं का प्रसार प्रतिरोध के साथ घटी हुई फिटनेस से प्रभावित हो सकता है, जो खासकर प्रतिजैविक के मौजूद नहीं होने की स्थिति में बैक्टीरिया को जीवित रखने में लाभप्रद साबित होता है। हालांकि, अतिरिक्त उत्परिवर्ती जीव (असानी से नष्ट हो जाने वाले) फिटनेस की कीमत की भरपाई और इन जीवाणुओं का अस्तित्व बहाल रखने में मदद कर सकते हैं।
अंतर्निहित आणविक प्रतिरोध तंत्र, जिससे प्रतिजैविक प्रतिरोध होता है, भिन्न-भिन्न हो सकता है। जीवाणु की आनुवंशिक बनावट के कारण मूलभूत प्रतिरोध स्वाभाविक है बैक्टीरियल गुणसूत्र उस प्रोटीन को एनकोड करने में विफल हो सकता है, जिसे प्रतिजैविक निशाना बनाता है। हासिल किया हुआ प्रतिरोध जीवाणु गुणसूत्र में परिवर्तन या अतिरिक्त गुणसूत्र डीएनए के अधिग्रहण से उत्पन्न होता है। प्रतिजैविक उत्पादित करने वाले जीवाणु सरल से जटिल बनने के प्रतिरोधक तंत्र का हिस्सा होते हैं, देखने में उनके जैसे ही होते हैं और प्रतिजैविक प्रतिरोधी उपभेदों में स्थानांतरित हो सकते हैं। प्रतिजैविक प्रतिरोध तंत्र का प्रसार क्षैतिज आनुवंशिक विनिमय द्वारा पिछली पीढ़ियों और डीएनए के आनुवंशिक पुनर्संयोजन से विरासत में मिले परिवर्तन के शीर्ष संचरण के माध्यम से होता है। प्रतिजैविक प्रतिरोध का प्लासमिड द्वारा विभिन्न जीवाणुओं के बीच विनिमय हो सकता है, जो जीवाणुरोधी प्रतिरोध को इनकोड करते हैं और जिससे एकाधिक प्रतिजैविक का सह अस्तित्व संभव होता है। ये प्लासमिड विविध प्रतिरोध तंत्र के साथ अलग जीन धारण किये हुए हो सकते हैं और असंबद्ध प्रतिजैविक से मिल सकते हैं, क्योंकि वे स्थानानांतरित किये गये एक प्रतिजैविक से ज्यादा प्लासमिड एकाधिक प्रतिजैविक प्रतिरोध पैदा करते हैं। वैकल्पिक रूप से बैक्टीरिया के भीतर अन्य प्रतिजैविक का आपसी प्रतिरोध तब होता है, जब चुने गये एक प्रतिजैविक से ज्यादा के प्रतिरोध के लिए जिम्मेवार वैसा ही प्रतिरोध तंत्र पैदा होता है।
प्रतिजैविक का दुरुपयोग
अनुपयुक्त प्रतिजैविक उपचार और प्रतिजैविक का अति प्रयोग प्रतिरोधी जीवाणुओं के उभरने का एक मुख्य कारक हैं। समस्या तब और जटिल हो जाती है, जब एक योग्य चिकित्सक के निर्देशों के बिना खुद प्रतिजैविक लेना शुरू करता है और कृषि में विकास प्रमोटरों के रूप में प्रतिजैविक का गैर-चिकित्सकीय उपयोग होता है। प्रतिजैविक दवाओं में बार-बार ये संकेत दिये जाते हैं कि कहां इनकी जरूरत नहीं हैं, या उपयोग गलत है या दिया गया प्रतिजैविक मामूली असर वाला है। यह कुछ वैसे मामलों में भी होता है, जहां संक्रमण बिना इलाज के भी ठीक हो सकता है। पेनिसिलिन और इरिथ्रोमाइसिन जैसे प्रतिजैविक, जो एक समय चमत्कारिक इलाज माने जाते थे, के अतिप्रयोग से 1950 के दशक के बाद से इनके प्रतिरोधक तत्व उभरने शुरू हो गये। अस्पतालों में प्रतिजैविक दवाओं के चिकित्सीय उपयोग को बहु-प्रतिजैविक प्रतिरोधी जीवाणुओं की वृद्धि के साथ जोड़ा जाता है।
प्रतिजैविक के दुरुपयोग के आम रूपों में-यात्रियों द्वाराप्रोफीलेटिक प्रतिजैविक का ज्यादा उपयोग, दवा लिखते समय रोगी के वजन व उसे पहले दी गयीं प्रतिजैविक दवाओं का ध्यान न रखना शामिल है, क्योंकि दोनों प्रतिजैविक दवाओं की प्रभावशीलता को नष्ट यहां तक कि पूरे कोर्स को विफल कर सकते हैं। ऐसा प्रतिजैविक लिखते समय उन्हें लेने के अंतराल (उदाहरण के लिए “हर 8 घंटे” पर या सिर्फ ” प्रति दिन 3x”) का उल्लेख नहीं करने, संक्रमित जीव के पूरी तरह स्वस्थ होने के लिए आराम का अभाव होने से भी प्रतिजैविक विफल हो सकते हैं। ऐसा करने से प्रतिजैविक प्रतिरोध के साथ जीवाणुओं की आबादी बढ़ने में मदद मिलेगी. अनुपयुक्त प्रतिजैविक उपचार प्रतिजैविक दुरुपयोग का एक आम रूप है। एक सामान्य उदाहरण के रूप में, हम आम सर्दी-जुकाम के लिए वायरल संक्रमण दूर करने वाली प्रतिजैविक दवाओं के इस्तेमाल को ले सकते हैं, जिसका उस पर कोई असर नहीं होता.श्वास नलिका के संक्रमण पर किये गये एक अध्ययन में पाया गया कि चिकित्सकों ने मरीजों के लिए उन्हीं प्रतिजैविक दवाओं को लिखा, जिनपर उनका विश्वास था, हालांकि वे हर 4 में से एक ही रोगी के उपयुक्त था। चिकित्सकों और मरीजों दोनों का बहुकार्यकारी हस्तक्षेप प्रतिजैविक दवाओं के अनुपयुक्त निर्धारण को कम कर सकता है। श्वास नलिका के संक्रमण का सहज निदान के लिए प्रतिजैविक दवाओं के लेने में 48 घंटे का विलम्ब प्रतिजैविक के इस्तेमाल को कम कर सकता हैं। लेकिन, यह रणनीति रोगी में संतोष की भावना कम कर सकती है।
रोगाणुरोधी प्रतिरोध से संबंधित कई संगठन विनियामक माहौल को बेहतर बनाने की पैरवी कर रहे हैं। अमेरिका के इंटरएजेंसी रोगाणुरोधी प्रतिरोध टास्क फोर्स की स्थापना का मकसद प्रतिजैविक दवाओं के दुरुपयोग और अतिप्रयोग से जुड़े मुद्दों से निपटने का प्रयास करना है, जिसका मकसद रोगाणुरोधी प्रतिरोध की समस्याओं का सक्रियता से अध्ययन करना है। अमेरिकी सेंटर फॉर डिजीज कंट्रोल एंड प्रिवेंशन, द फूड एंड ड्रग एडमिनिस्ट्रेशन (FDA), नेशनल इंस्टीट्यूट ऑफ हेल्थ (NIH) तथा कई अन्य सरकारी एजेंसियां इन मुद्दों पर विचार के लिए आपस में समन्वय रखती हैं।
एक गैर सरकारी संगठन अभियान समूह का नाम “कीप प्रतिजैविक वर्किंग” है। फ्रांस में 2002 से एक सरकारी अभियान “एंटीबायोटिक्स आर नॉट ऑटोमैटिक” शुरू किया गया है, जिससे अनावश्यक प्रतिजैविक नुस्खों, खासकर बच्चों के लिए, में कमी आई है। यूनाइटेड किंगडम में, कई डॉक्टरों के क्लिनिकों में NHS पोस्टर लगाए गए हैं, जिनमें संकेत किया गया है कि ‘दुर्भाग्य से, प्रतिजैविक दवाओं की कितनी भी मात्रा आपको सर्केदी से छुटकारा नहीं दिला सकती, क्योंकि कई रोगी अपने डाक्टर से खासकर अनुपयुक्त प्रतिजैविक देने का अनुरोध करते है, इस विश्वास से उन्हें वायरल संक्रमण के इलाज में मदद मिलेगी.
कृषि में, पशुओं में वृद्धि-प्रायोजकों के रूप में प्रतिजैविक दवाओं के गैर-निदानमूलक उपचार के साथ संबद्ध प्रतिजैविक प्रतिरोध 1970 में ब्रिटेन में (Swann 1969 की रिपोर्ट) के बाद प्रतिबंधित रूप में शुरू हुआ। वर्तमान में पूरे यूरोपीय संघ में विकास प्रायोजकों के रूप में प्रतिजैविक दवाओं के गैर-निदानमूलक उपयोग पर पाबंदी लगी है। अनुमान किया जाता है कि अमेरिका में प्रयुक्त प्रतिजैविक दवाओं का 70% से अधिक हिस्सा रोग हुए बिना ही जानवरों (मुर्गी, सुअर और पशु) को खिला दिया जाता है। खाद्य पशु उत्पादन में प्रतिजैविक के उपयोग साल्मोनेला spp, कैपीलोबैक्टर एसपीपी, एसचेरिचिया कोलाई और इंट्रोकुकस एसपीपी सहित जीवाणुओं के प्रतिरोधी प्रकारों से जुड़ा हुआ है। कुछ अमेरिकी साक्ष्यों और यूरोपीय अध्ययनों से संकेत मिलता है कि ये प्रतिरोधी बैक्टीरिया इंसानों में संक्रमण का कारण बनते हैं, जो सामान्यतः निर्धारित प्रतिजैविक के प्रति कोई प्रतिक्रिया नहीं देते. इन रिवाजों और संबद्ध समस्याओं के संबंध में कई संगठन, जैसे (अमेरिकन सोसाइटी फॉर माइक्रोबायोलॉजी-ASM, अमेरिकन पब्लिक हेल्थ एसोशियेशन-APHA और अमेरिकन मेडिकल एसोसिएशन-AMA) ने खाद्य पशुओं के उत्पादन में प्रतिजैविक के उपयोग पर प्रतिबंध लगाने और इसका सभी तरह गैर-चिकित्सीय प्रयोग खत्म करने की जरूरत बताई है।हालांकि, प्रतिजैविक दवाओं के उपयोग को सीमित करने के लिए विनियामक और विधायी कार्रवाई में देरी आम है और इसमें इन प्रतिजैविक का उपयोग कर रहे या बेच रहे उद्योगों का विरोध और साथ-साथ प्रतिजैविक के उपयोग और विषाणुजनित लाइलाज बीमारियों के बीच आकस्मिक संपर्क बनाने से संबंधित अनुसंधान में लगे उद्योगों का विरोध भी शामिल हो सकता है। दो संघीय विधेयक (S.742 और H.R.2562, जिनका लक्ष्य चरणबद्ध रूप से अमेरिकी खाद्य पशु उत्पादन गैर-निदानमूलक उपचार में प्रतिजैविक दवाओं के प्रयोग को खत्म करना था, प्रस्तावित तो किये गये, पर इन्हें पारित नहीं किया जा सका. इन विधेयकों का अमेरिकन होलिस्टिक नर्सेज एसोसिएशन, द अमेरिकन मेडिकल एसोसिएशन और द अमेरिकन पब्लिक हेल्थ एसोसिएशन (APHA) सहित जन स्वास्थ्य और मेडिकल संगठनों ने समर्थन किया था। यूरोपीय संघ ने 2003 के बाद से विकास संवर्द्धक एजेंट के रूप में प्रतिजैविक दवाओं के इस्तेमाल पर प्रतिबंध लगा दिया है।
प्रतिरोध को संशोधित करने वाले एजेंट
वर्तमान में प्रतिरोध का सामना करने के दवा यौगिकों के विकास के लिए एक समाधान पर अनुसंधान किया जा रहा है, जो कई प्रतिजैविक प्रतिरोध को वापस कर सकता है। ये तथाकथित प्रतिरोध को संशोधित करने वाले एजेंट MDR तंत्र को निशाना बना सकते हैं और उन्हें बाधित कर सकते हैं, जिससे बैक्टीरिया प्रतिजैविक दवाओं से आक्रांत हो सकते हैं, जो पहले से ही प्रतिरोधी के रूप में मौजूद थे। ये यौगिक अन्य सहित निम्नांकित को निशाना बना सकते हैं-
- बहिःस्त्रवण अवरोधन (Phe-Arg-β-naphthylamide)
- बीटा लैक्टामास इनहिबिटर्स- क्लावुलैनिक एसिड और सलबैक्ट्रम के साथ शामिल
प्रतिजैविक दवाओं से परे: गैर-बैक्टीरिया संक्रमण का इलाज[संपादित करें]
|
|
इस section के विषय पर किसी विशेषज्ञ के ध्यान की जरूरत हैं। जानकारी के लिए वार्ता पृष्ठ देखें। विकिपरियोजना Pharmacology विशेषज्ञ की भर्ती में मदद करने में सक्षम हो सकता है। (जुलाई 2009) |
|
|
इस भाग से या तो उद्धरण अनुपस्थित हैं या उनके स्रोतों की आवश्यकता है। कृपया उद्धरण जोड़कर कॉपीराइट उल्लंघन और तथ्यात्मक त्रुटियों से लेख की रक्षा करें। (अक्टूबर 2009) |
यौगिकों की पहचान के तुलनात्मक अध्ययन, जो सुरक्षित रूप से बैक्टीरिया का संक्रमण ठीक करता है, कवक और वायरल संक्रमण के उपचार में नकली की पहचान करना मुश्किल था। प्रतिजैविक अनुसंधान से जैव रसायन के ज्ञान के क्षेत्र में काफी प्रगति हुई और इससे बैक्टीरियल सेल के सेलुलर और आणविक शरीर विज्ञान के बीच बड़े मतभेद पैदा हुए और यही बात स्तनधारी सेल के संबंध में हुई. इससे इस राय की व्याख्या हुई कि कई यौगिक जो बैक्टीरिया के लिए भले ही विषाक्त हों, पर वे मानव कोशिकाओं के प्रति अ-विषाक्त हैं। इसके विपरीत, कवक प्रकोष्ठ के बुनियादी जैव रसायन (बायोकेमेस्ट्रीज) और स्तनपायी सेल काफी कुछ मिलते-जुलते हैं। यह चिकित्सीय यौगिकों के विकास और प्रयोग को कवक सेल पर हमले पर केंद्रित रखता है, जबकि स्तनपाई कोशिकाओं को नुकसान नहीं पहुंचाता. वायरल रोगों के प्रतिजैविक इलाज में इसी तरह की समस्याएं दिखती हैं। मानव वायरल चयापचय जैव रसायन मानव जैव रसायन के बहुत समान है और एटीवायरल यौगिकों के संभावित निशाने बहुत कुछ एक स्तनधारी वायरस के लिए अद्वितीय घटक तक ही सीमित रह जाते हैं।
संबंधित लेखों के लिए, फंगीसाइड, ऐंटिफंगल दवाएं और एंटीवायरल दवा देखें.
प्रतिजैविक दवाओं से परे : बहु-औषधि प्रतिरोधी बैक्टीरिया का इलाज
बहु-औषधि प्रतिरोधी जीवों (MDRO) का मतलब आम तौर पर उस बैक्टीरिया से निकाला जाता है, जो क्लासिकल प्रतिजैविक दवाओं की नैदानिक खुराक, जिन्हें हाल ही में उनके निदान के लिए लिया गया हो, को प्रभावित नहीं कर रहे हैं। इन जीवों की वृद्धि से वैकल्पिक जीवाणुरोधी उपचार की जरूरत पैदा हुई है।
फेज चिकित्सा, जिसके तहत बैक्टीरिया पर हमले के लिए खास तरह के वायरसों का प्रयोग किया जाता है, 1920 और 1930 के दशक के दौरान अमेरिका, पश्चिमी और पूर्वी यूरोप में उपयोग में थी। फेज आसपास की पारिस्थितिकी में पैदा हुआ बैक्टीरिया का एक आम अंग हैं, जो आंत, सागर, मिट्टी और अन्य वातावरण में जीवाणुओं की जनसंख्या पर काफी नियंत्रण रखता है। इन उपचारों की सफलता काफी हद तक अनुमान या कल्पना पर आधारित या खराब तरीके से नियंत्रित है।
मूल प्रकाशन भी सामान्य तौर पर अबूझ बने हुए हैं, यहां तक कि रूसी भाषा के पंडित भी इन्हें नहीं पढ़ सकते. 1940 के दशक में पेनिसिलिन के आविष्कार के साथ ही यूरोप और अमेरिका ने प्रतिजैविक दवाओं के इस्तेमाल की चिकित्सीय रणनीति ही बदल दी. हालांकि, पूर्व सोवियत संघ में फेज उपचार के संबंध में अध्ययन जारी था। जॉर्जिया के गणराज्य में एलिवा इंस्टीट्यूट ऑफ बैक्टीरियोफेज, माइक्रोबायोलोजी एवं वायरोलोजी द्वारा फेज उपचार के प्रयोग पर अनुसंधान जारी है। विभिन्न कंपनियां (अन्य के अलावा इंट्रालिटिक्स), विश्वविद्यालय व उत्तरी अमेरिका और यूरोप के फाउंडेशन वर्तमान में फेज चिकित्सा पर शोध कर रहे हैं।[कृपया उद्धरण जोड़ें][65] हालांकि, वायरसों को स्वतंत्र रूप से छोड़ देने की जेनेटिक इंजीनियरिंग के बारे में चिंता की वजह से वर्तमान में फेज चिकित्सा के कुछ पहलुओं को सीमित ही मानना चाहिए. एक परिणाम के लिए फेज का उपयोग अन्य तरीके से सीधे बैक्टीरिया को संक्रमित करने का प्रयास है।[66][67] जबकि बैक्टीरियोफेज और संबंधित चिकित्सा प्रतिजैविक प्रतिरोध के पहलुओं का एक संभावित समाधान प्रदान करते हैं, चिकित्सकीय इलाज में उनका स्थान अब भी सवालों के घेरे में है।[कृपया उद्धरण जोड़ें]
“बैक्टीरियोसिन” भी क्लासिक छोटे अणु प्रतिजैविक के बढ़ते हुए विकल्प हैं। बैक्टीरियोसिन्स के विभिन्न वर्गों के चिकित्सकीय एजेंट के रूप में विभिन्न तरह की संभावनाएं हैं। छोटे अणु बैक्टीरियोसिन्स (उदाहरण के लिए मोइक्रोसिन्स और लैंटीबायोटिक्स) क्लासिक प्रतिजैविक दवाओं के समान ही सकते हैं; कोलिसिन की तरह बैक्टीरियोसिन्स के अधिक संकुचित स्पेक्ट्रम के होने की संभावना हैं, जिससे चिकित्सा करने से पहले नये आण्विक निदान की मांग पैदा होगी और इससे उसी स्तर पर प्रतिरोध की आशंका हीं बढ़ायेगा. बड़े अणु प्रतिजैविक दवाओं का एक दोष यह है कि उनके लिए मेंबरेन (झिल्ली) को पार करने और पूरे शरीर में प्रणालीबद्ध रूप से यात्रा करने में सापेक्ष कठिनाई होती है।
इस कारण से, वे सबसे अधिक स्थानीय या आंत के जरिये प्रयोग के लिए प्रस्तावित किये जाते हैं क्योंकि बैक्टीरियोसिन्स पेप्टाइड हैं, वे और अधिक आसानी से छोटे अणुओं की तुलना में सक्रिय हो सकते हैं।[70] इससे कॉकटेल और गतिशीलता से संवर्द्धित किये गये प्रतिजैविक दवाओं की पीढ़ी के पैदा होने की अनुमति दे सकते हैं, जिनमें प्रतिरोध से उबरने की क्षमता पैदा होती हैं।
पोषक तत्वों की वापसी प्रतिजैविक को बदलने या उनका पूरक विकल्प तैयार करने की एक संभावित रणनीति हो सकती है। लौह तत्व की उपलब्धता पर पाबंदी एक तरीका है, जिससे मानव शरीर जीवाणु प्रसार को सीमित किया जा सकता है। शरीर को लौह मुक्त करने का तंत्र (जैसे विषाक्त पदार्थ और साइड्रोफारेस) रोगजनकों के बीच आम है। ये गतिशील, विभिन्न शोध समूह नये तरह के शोधकों (केलेशर्न्स) को पैदा करने के प्रयास में हैं, जो लौह तत्व को वापस खींच लेंगे, अन्यथा ये रोगजनकों बैक्टीरिया कवक और परजीवी के लिए उपलब्ध हो जायेंगे. यह जीवाणु संक्रमण, अत्यधिक लौह तत्व के सफल उपचार सहित, से अलग स्थितियों के लिए की जाने वाली केलेशन थेरेपी से अलग है।
MDRO संक्रमणों के मुकाबले के लिए आम तौर पर टीके का सुझाव दिया जाता है। वे वास्तव में चिकित्सा के एक बड़े वर्ग के भीतर समा जाते हैं, जो प्रतिरक्षा मॉड्यूलेशन या वृद्धि पर निर्भर होते हैं। ये चिकित्सा प्रणालियां संक्रमित या संभावित मेजबान की प्राकृतिक प्रतिरोधक क्षमता को जगाती हैं या मजबूत बनाती हैं, जिससे मैक्रोफेज, एंटीबॉडी का निर्माण, सूजन, या अन्य क्लासिक प्रतिरक्षा प्रतिक्रिया जैसी गतिविधियां दिखती हैं।
क्योंकि, मैक्रोफेज बैक्टीरिया को भस्म करता है और उन्हें लील जाता है, बॉयोथेरेपी के विभिन्न रूपों का सुझाव दिया जाता है, जो जीव को रोगजनकों को लील जाने के लिए तैयार करते हैं। इसमें प्रोटोजोआ की तैनाती और मैगेट ेरेपी शामिल हैं।
प्रोबायोटिक एक अन्य विकल्प है, जो एक लाइव कल्चर पैदा कर पारंपरिक प्रतिजैविक से आगे जाता है, जो सिद्धांत रूप में अपने आपको एक स्यामबायंट, प्रतिस्पर्धी, बाधा, निवास करने या साधारण रूप से रोगजनकों के औपनिवेशीकरण में हस्तक्षेप करनेवाले साबित करते हैं।